CD-Labor für Krebsimmuntherapie mit pharmakologischem NR2F6 Inhibitor
Leitung
Unternehmenspartner
Laufzeit
01.04.2019 - 31.03.2020
Thematischer Cluster

Mit der Krebsimmuntherapie werden derzeit große Hoffnungen verbunden, sie steckt aber noch in den Kinderschuhen. Dieses CD Labor beschreitet nun völlig neue Wege um dem Körper zu ermöglichen, sich selbst gegen den Tumor zu wehren.
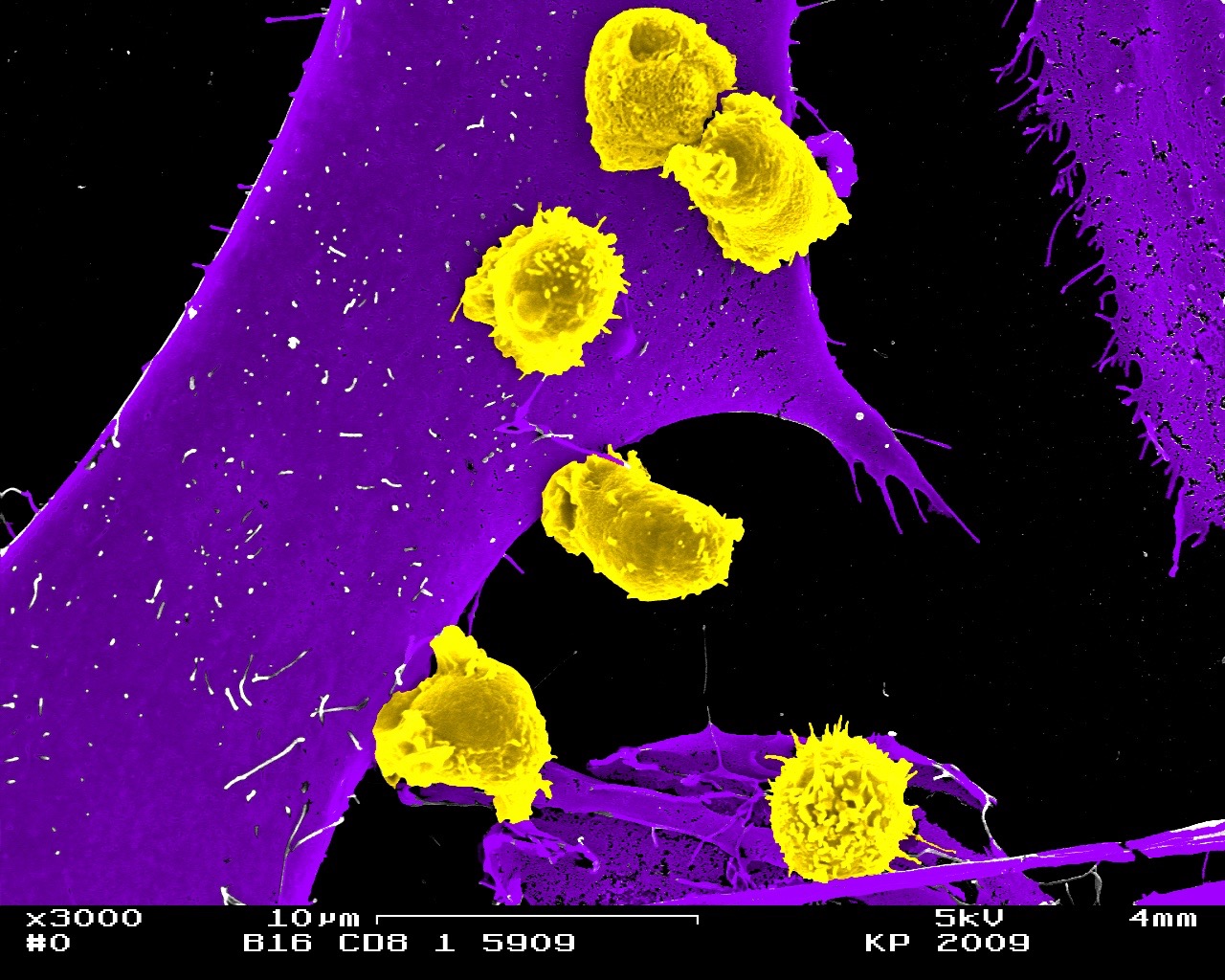
Das Immunsystem ist dafür ausgerüstet, Krebszellen zu erkennen und zu eliminieren. Es gibt allerdings hemmende Rezeptoren und Liganden, die das Immunsystem in Schach halten, die sogenannten Immune Checkpoints oder Immunkontrollpunkte. Dies geschieht beim gesunden Menschen, um zu verhindern, dass es im Laufe einer Immunantwort zu Schädigungen der umgebenden Gewebe oder gar zu Autoimmunreaktionen kommt. Krebszellen können jedoch diese Immunkontrollpunkte und ihre Mechanismen kapern und so ihre Zerstörung durch das Immunsystem umgehen. Neueste Krebstherapien setzen nun genau an diesen Immunkontrollpunkten an. Sie versetzen den Körper in die Lage, den Krebs durch körpereigene Abwehrzellen, sogenannte T-Zellen, richtiggehend aufzulösen.
Dieses CD Labor widmet sich der Erforschung des Immunkontrollpunkts NR2F6. Im Gegensatz zu anderen Ansätzen im Bereich der Immunkontrollpunkte, wo teure synthetische Antikörper an den Immunkontrollpunkten PD-1 und CTLA-4 an der Zelloberfläche binden, befindet sich NR2F6 im Zellinneren, genauer im Zellkern, und kann mit „small molecule drugs“ oder niedermolekularen Wirkstoffen pharmakologisch gehemmt werden. Solche neuartigen Medikamente bieten daher eine vielversprechende und von Krankenkassen bezahlbare Chance, Krebserkrankungen bei guter Lebensqualität der Betroffenen und über lange Zeit beherrschen zu können.
Die Forschungsarbeit gliedert sich dabei in zwei Bereiche. Im ersten Forschungsbereich soll zum einen das Grundlagenwissen über die Bedeutung und Funktion von NR2F6 erweitert werden. Man hat erste Hinweise, dass NR2F6 als Biomarker für die Tumorerkennung eingesetzt werden könnte, da NR2F6 bei manchen Patienten stark hochreguliert ist. Für den Einsatz als Tumormarker muss NR2F6 jedoch weiter studiert und validiert werden. Weiters gibt es Hinweise, dass die Hemmung von NR2F6 die Wirksamkeit der Antikörper zur Hemmung von PD-1 und CTLA-4 erhöhen und somit zu einer Einsparung dieser teuren Wirkstoffe führen könnte. Letztlich werden zwei Verfahren zur Hemmung von NR2F6 miteinander verglichen, nämlich die pharmakologische Hemmung durch kleine Moleküle mit der auf RNA-Interferenz (siRNA; small interfering ribonucleic acid) basierenden Hemmung. siRNA bindet an die NR2F6 mRNA und hemmt so die Expression dieses Gens.
Im zweiten Forschungsbereich geht es um die Entdeckung von Arzneistoffen, welche NR2F6 hemmen können. Hier muss zuerst verstanden werden, welche Molekülklassen strukturell für eine Hemmung in Frage kommen und wie diese Hemmung genau vonstattengeht. Auf Basis dieses Wissens können neue Moleküle gezielt designt und besonders wirksame Moleküle identifiziert werden (Hit-to-lead development). Weiters sollen natürliche Liganden identifiziert werden, welche NR2F6 im Rahmen seiner natürlichen Funktionen binden und diese regulieren. Der natürliche Ligand von NR2F6 ist derzeit noch nicht bekannt. Schließlich sollen die Moleküle, welche sich in vorangegangenen Forschungsschritten als die wirksamsten herausgestellt haben (Lead Compounds) in Mausmodellen getestet werden.
Dieses CD-Labor macht sich auf die Suche nach einem völlig neuartigen Krebsimmunwirkstoff, welcher die Menschheit möglicherweise einen Schritt näher zur Heilung zumindest einiger Krebsarten führen könnte.
Christian Doppler Forschungsgesellschaft
Boltzmanngasse 20/1/3 | 1090 Wien | Tel: +43 1 5042205 | Fax: +43 1 5042205-20 | office@cdg.ac.at

